

单B细胞筛选平台的目标是从天然免疫库中直接获得细胞水平已被选择过的抗体序列组合,并尽可能保留重链与轻链的天然配对关系。与依赖随机组合的展示文库不同,该平台以抗原特异性B细胞为起点,将细胞表面结合事件转换为可分选的荧光信号,再将单细胞中的可变区转写并扩增为可用于重组表达的序列信息。平台性能通常由三类因素共同决定:抗原特异性识别的准确性、单细胞分选的纯度与回收效率、以及单细胞扩增对VH/VL配对关系的保持程度。
单B细胞筛选的第一步是将“抗原结合”转化为可测的荧光信号。常见策略是使用带荧光基团的重组抗原作为探针,与B细胞表面BCR发生结合后使目标细胞在相应通道出现信号。为降低非特异性吸附或荧光标签相关的假阳性,实践中常采用双标抗原策略,即同一抗原分别连接两种不同荧光基团,在分选时要求细胞在两个抗原通道同时呈阳性,从而提高特异性判定的稳健性。为避免将死细胞或细胞碎片带入下游扩增,通常还会加入活性染料或排除性标记,并结合散射信号排除低质量事件。上述策略的核心是明确区分BCR-抗原特异性结合信号,从源头提高后续VH/VL回收的有效比例。
流式细胞分选在该平台中承担“从群体到单细胞”的关键转化。多参数门控通常包含三类信息:细胞质量控制(如双ts/聚集体排除、活细胞筛选)、B细胞谱系标记(如CD19/CD20等)与抗原结合信号(单标或双标抗原通道)。
对于免疫后样本,还可加入免疫球蛋白同种型标记以富集IgG记忆B细胞相关群体,从而提高获得亲和力成熟序列的概率。分选过程将符合门控条件的事件以单细胞形式沉积到96孔或384孔板,或直接进入单细胞反应体系。该步骤的技术重点在于门控逻辑的一致性与分选纯度控制:门控过宽会显著增加非特异性细胞比例,门控过窄则会降低回收率并偏向高信号亚群,影响序列多样性覆盖。
单细胞尺度下mRNA含量极低,序列回收对降解高度敏感,因此分选后的裂解与稳定化是影响成功率的决定环节。常见做法是在收集体系中预置温和裂解条件并加入RNase抑制体系,使裂解后核酸能在短时间内保持可用于反转录。随后通过反转录获得cDNA,并以针对免疫球蛋白可变区或恒定区保守序列的引物进行扩增。
为提高回收率并降低非特异性扩增,嵌套PCR常用于单细胞扩增流程,通过两轮扩增提高目标片段的富集程度。该阶段的核心控制点是样本处理的一致性与反应体系的抑制因素管理,使“单细胞差异”不被“前处理差异”放大为系统偏差。
单B细胞平台的关键优势在于能够保留VH与VL的天然配对关系。由于重链与轻链在单个B细胞内同时转录与表达,单细胞分选将两者天然共存于同一反应体系,为配对回收提供了物理前提。常见的实现路径是对同一孔内的重链与轻链分别扩增,并将扩增产物用于后续克隆与表达构建,从而在样本层面保留配对关系。对于更强调配对锁定的平台,可采用在同一反应体系内实现重轻链产物的连接策略,或在后续建库过程中引入配对保持的连接设计,使VH与VL以“同一分子标签”或“同一扩增产物”的形式进入测序或表达构建环节。无论采用何种方式,评价重点都应回到两类结果:其一,是否能够在较高比例的单细胞中同时获得VH与VL完整可变区序列;其二,回收的VH/VL组合是否能够在重组表达后维持与原始细胞一致的结合特异性与基本功能表现。
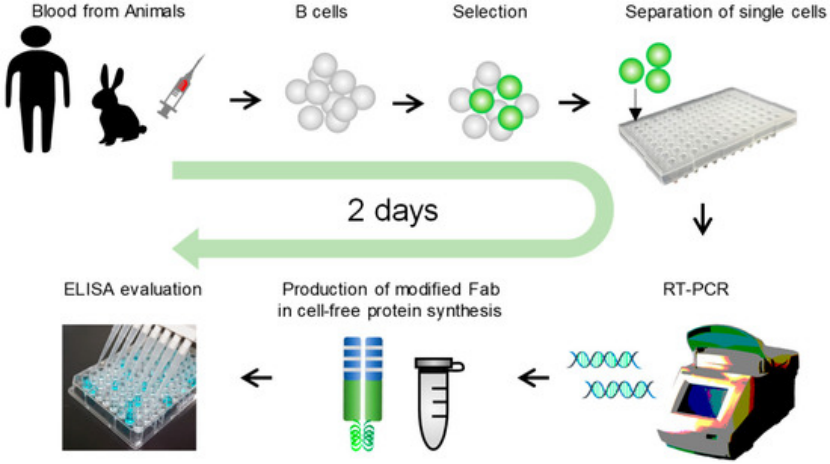
单B细胞筛选平台的分子基础可概括为三条连续链路:抗原探针将特异性结合事件转化为可分选信号;多参数流式分选在群体中富集并沉积单个抗原特异性B细胞;单细胞裂解、反转录与扩增在低模板条件下获得可变区序列,并在单细胞层面保留VH/VL天然配对关系。