

杂交瘤平台用于将“抗体特异性”与“持续增殖能力”整合到同一细胞体系中。其基本思路是以免疫动物获得的抗原特异性B细胞作为可变区序列来源,以骨髓瘤细胞提供持续分裂能力,通过体细胞融合形成可长期培养的分泌细胞群,并借助代谢选择压力与克隆化步骤获得序列与分泌行为高度一致的单克隆抗体。该体系的关键不在于单一操作环节,而在于融合、生存选择与克隆均一性三类机制的相互配合。
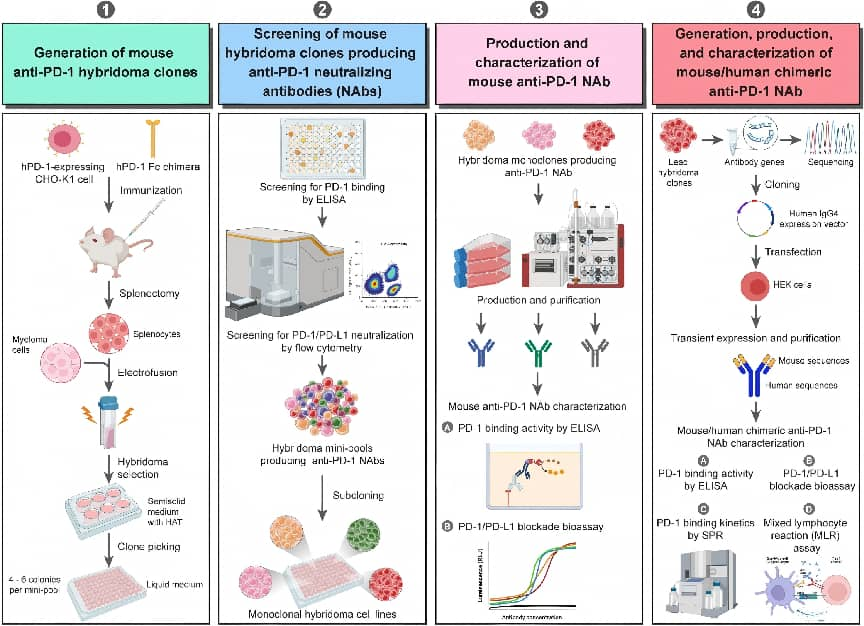
杂交瘤技术的起点是免疫后获得的B细胞群体。抗原进入机体后,B细胞通过BCR识别表位并在免疫微环境中完成克隆扩增与亲和力成熟,形成具有特异性免疫球蛋白序列的分泌细胞谱系。
就分子层面而言,单个B细胞对应一组确定的重链与轻链可变区序列,因此其分泌抗体具有明确的序列边界与结合特异性。限制因素在于原代B细胞离体后增殖能力有限,难以维持长期稳定分泌;杂交瘤平台通过引入可无限增殖的骨髓瘤细胞来解决这一持续性问题,从而把特异性序列“固化”为可传代的细胞遗传状态。
体细胞融合的目标是形成同时具备分泌与增殖特征的杂交细胞。常见融合诱导条件包括PEG介导融合或电融合,其共同点是暂时性改变细胞膜的物理化学状态,使两类细胞的脂质双层在近距离接触后发生膜重排并形成连续膜结构。
以PEG为例,PEG可降低细胞表面水化层稳定性并削弱细胞间排斥,使膜接触概率上升;随后在去PEG与膜恢复过程中,局部膜融合可形成异核体,继而在细胞周期推进中完成核融合与遗传物质的共同维持。融合体系中会同时存在未融合亲本细胞、同源融合体与目标杂交细胞,因此后续必须通过代谢选择策略将目标群体从混合体系中分离出来。
HAT筛选的核心在于将细胞存活与核苷酸合成路径绑定,从而在混合群体中选择出特定代谢能力组合的细胞。细胞合成嘌呤与嘧啶核苷酸可通过从头合成途径与补救合成途径两条路径完成。HAT培养基中使用氨基蝶呤抑制叶酸循环相关酶系,导致从头合成途径受阻;与此同时,培养基补充次黄嘌呤与胸腺嘧啶,为补救合成途径提供底物。用于融合的骨髓瘤细胞通常带有HGPRT或TK相关缺陷,使其无法有效利用补救合成途径,因此未融合骨髓瘤细胞在HAT条件下无法维持增殖。
未融合B细胞虽具备补救合成能力,但其离体存活与增殖能力有限,亦难以长期维持。只有融合后获得B细胞来源补救合成能力、同时保留骨髓瘤细胞增殖特征的杂交细胞,能够在HAT培养基中持续存活并形成可扩增群体。该选择体系的意义在于以明确的代谢约束实现细胞类型筛选,而不是依赖形态学或非特异性筛除。
获得HAT存活群体后,下一关键步骤是克隆化以确保单克隆性。有限稀释的原则是将细胞悬液稀释到单位孔内的期望细胞数低于1,使多数孔为空孔,少数孔由单个细胞起始形成克隆。该方法的核心是以泊松分布描述接种后每孔细胞数的概率,从统计上提高单细胞起源孔的比例,并通过后续复筛进一步降低多细胞起源导致的混合克隆风险。克隆建立后,常以ELISA对分泌抗体进行特异性与结合能力评估,并结合生长与分泌稳定性指标筛选适合扩增的候选克隆。
杂交瘤平台以体细胞融合将B细胞的抗体特异性与骨髓瘤细胞的持续增殖能力整合为稳定遗传状态,并通过HAT培养基对核苷酸补救合成途径的选择性约束实现目标群体富集,随后以有限稀释完成单细胞起源克隆建立,并通过ELISA等分析手段完成分泌特异性评估。基于哺乳动物细胞内折叠与修饰背景,杂交瘤来源IgG通常具备较一致的重轻链配对与结构加工特征,为获得高度均一的单克隆抗体提供了可解释的细胞学与代谢学基础。